METABOLISMO HEPÁTICO Y VACA EN TRANSICIÓN
Adrian González Garrido. Departamento de Rumiantes. NUTRAL SA
Vaca en transición, fase de periparto, lotes preparto/postparto: las tres expresiones significan lo mismo y engloban probablemente una de las fases más apasionantes del ciclo productivo de la vaca de leche de alta producción desde muy diferentes puntos de vista. Conocer y controlar todo lo que acontece en esta etapa supondrá tener éxito en la siguiente lactación, alcanzando muy altas producciones sin mermar la capacidad reproductiva ni el estado de salud de las vacas.  Dominar el periparto se ha convertido en una maravillosa obsesión para los nutricionistas puesto que supone colocar a las vacas en la línea de salida de la gran carrera productiva, con los motores en marcha y el tanque lleno de gasolina (¿o de leche?). No nos equivocaremos mucho si nos atrevemos a afirmar que los establos más rentables del mundo son, y serán cada vez más en el futuro, aquellos que consigan a través de un buen manejo y alimentación reducir hasta la nulidad los problemas que aparecen durante las primeras semanas posteriores al parto.
Dominar el periparto se ha convertido en una maravillosa obsesión para los nutricionistas puesto que supone colocar a las vacas en la línea de salida de la gran carrera productiva, con los motores en marcha y el tanque lleno de gasolina (¿o de leche?). No nos equivocaremos mucho si nos atrevemos a afirmar que los establos más rentables del mundo son, y serán cada vez más en el futuro, aquellos que consigan a través de un buen manejo y alimentación reducir hasta la nulidad los problemas que aparecen durante las primeras semanas posteriores al parto.
El periparto o “período alrededor del parto” engloba las tres a cuatro semanas antes y después del parto, y supone para la vaca un cambio metabólico repentino y de gran magnitud que es más acusado cuanto mayor potencial genético tiene la vaca: una mala gestión de esta fase ligado a animales de alto rendimiento provoca irremediablemente la aparición de un gran número de patologías con costes altísimos para el ganadero. La denomina- ción del periparto como fase de vaca en transición es también muy acertado puesto que pone de relieve la realidad de la vaca de pasar de una fase metabolicamente más tranquila con pocas necesidades nutricionales (últimas semanas de gestación) a una fase, que se inicia inmediatamente después del parto, donde la glándula mamaria provoca una explosiva demanda de nutrientes que obliga al meabolismo a trabajar al 100 % en pocos días; para hacer frente a este cambio la vaca debe estar preparada; esta preparación debe iniciarse antes del parto y persigue lo que se ha bautizado como la transición de la vaca de leche. Esta nueva filosofía de trabajo sólo puede ha- cerse cuando en los establos disponemos de sitio para separar físicamente las vacas antes y después de parir, es decir, donde podemos hacer lotes de preparto y post- parto.
La razón práctica de darle tanta prio- ridad al periparto se basa, como siempre, en el estudio de los números: la gran ma- yoría de los patologías que nos encontra- mos en las explotaciones se producen durante los 30 a 60 primeros días de lactación y esta demostrado que tiene una relación directa con la fase de transición. Muchas de estas patologías no son mortales pero provocan tantos daños en las vacas que a corto/medio plazo terminan en el matadero; es decir, no sufren una muerte natural pero terminamos matándolas antes de tiempo; probablemente esta sea una de las razones de fondo de los elevados índices de reposición de las vaquerías de todo el mundo y pone de relieve una gran problemática que cuesta mucho dinero al ganadero, tanto por costes de tratamientos como por bajas de los mejores animales de la explotación. Debemos pensar que esta problemática es evitable, que debemos obligar al ganadero a desarrollar unas buenas prácticas de manejo del periparto y establecer nosotros, como profesionales que le asesoramos, una serie de medidas concretas de control.
Pero, ¿qué ocurre durante el periparto para que sea una fase de tan alto riesgo? Podemos resumirlo en cuatro grandes eventos:
1.- Se incrementa la actividad del hígado
al movilizar la vaca tras el parto grandes cantidades de grasa como fuente de energía.
2.- Se produce un cambio muy importante en la mucosa y en el microbismo ruminal como consecuencia del cambio de dietas de preparto a postparto.
3.- Hay una fuerte demanda de calcio por parte de la glándula mamaria que obliga a la vaca a incrementar repentinamente los niveles séricos de calcio para mantener la actividad muscular.
4.- La vaca sufre durante el periparto una importante bajada de defensas (inmunosupresión) cuya magnitud esta estrechamente ligado al grado de estrés que deba soportar durante esta fase.
Todos estos cambios son importantes y deben ser vigilados; el fallo en uno de ellos puede hacer fracasar el esfuerzo realizado en los otros; en muchas ocasiones se producen errores en varios de ellos simultáneamente lo que provoca la aparición de varias patologías al mismo tiempo que dificulta el diagnóstico de la causa primaria. Todas estas apreciaciones y muchas más que podríamos citar ponen de relieve la enorme complejidad de esta fase del 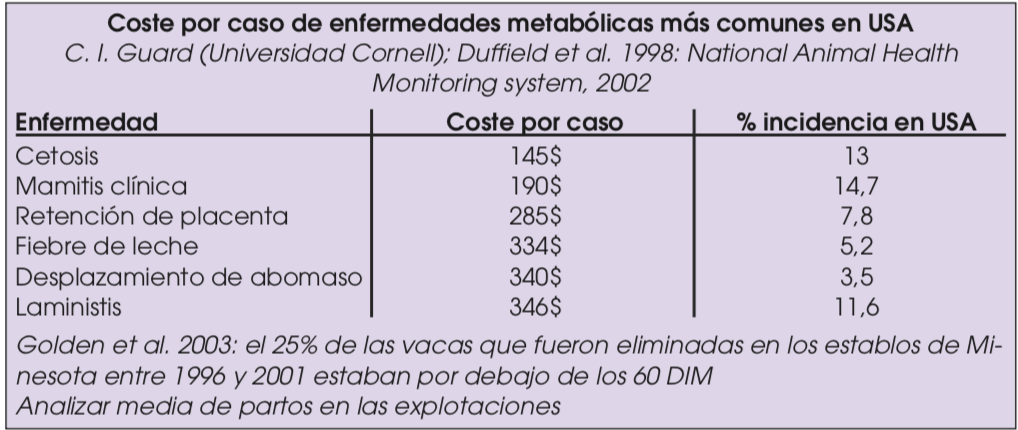 ciclo productivo y su importancia. Dominar y controlar cada aspecto es esencial para establecer un buen plan de transición. Dado que es materialmente imposible abarcar los cuatro puntos en un mismo artículo, trataremos de explicar lo mejor posible al menos el primero de ellos, tal vez el más importante de todos.
ciclo productivo y su importancia. Dominar y controlar cada aspecto es esencial para establecer un buen plan de transición. Dado que es materialmente imposible abarcar los cuatro puntos en un mismo artículo, trataremos de explicar lo mejor posible al menos el primero de ellos, tal vez el más importante de todos.
METABOLISMO HEPÁTICO Y VACA EN TRANSICIÓN
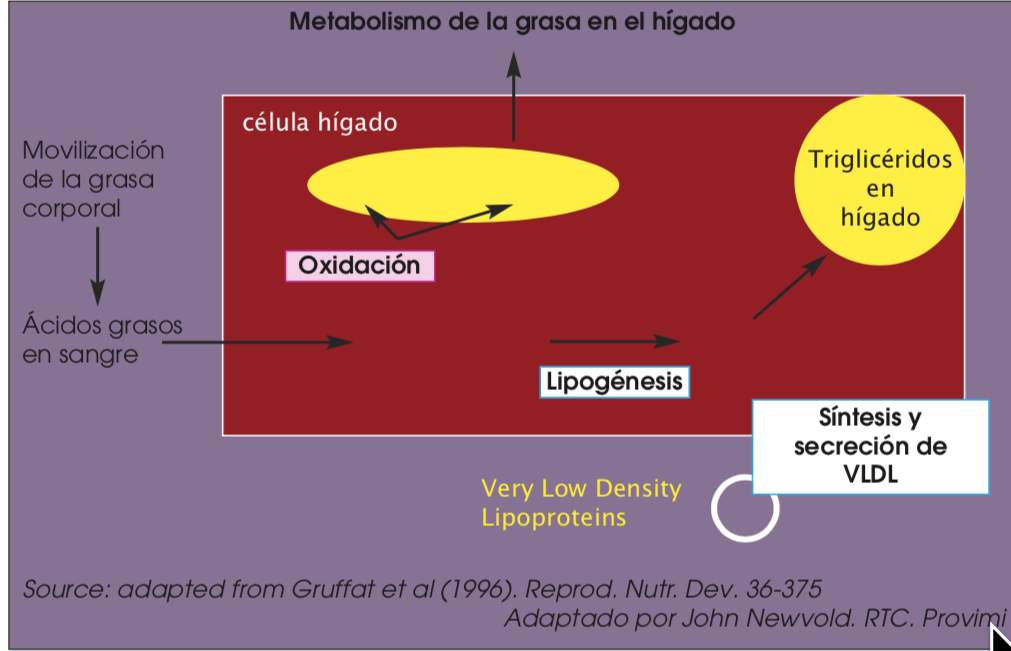
Como decíamos al principio, el período de periparto en el ciclo productivo de la vaca en lactación esta caracterizado por cambios dramáticos en la de- manda de nutrientes que necesitan una exquisita coordinación metabólica para cubrir los requerimientos en energía, glucosa y aminoácidos por la glándula mamaria después del parto. Para cubrir las necesidades en energía durante las primeras semanas de lactación, la vaca de leche moviliza una gran cantidad de ácidos grasos procedentes de las reservas del tejido adiposo, dando como resultado el incremento de la concentración de ácidos grasos no esterificados o NEFA (sus siglas en inglés). Los NEFA son utilizados por los tejidos periféricos como fuente de energía, incorporados a la leche y también extraídos por el hígado desde la corriente sanguínea en proporción directa a los NEFA que llegan. Los NEFA extraídos por el hígado son oxidados (“quemados” para obtener energía) o esterificados en triglicéridos para ser exportados del hígado como lipoproteínas de muy baja densidad (VLDL) o bien almacenados en el hígado. La capacidad del hígado de los rumiantes para oxidar los NEFA o exportarlos como VLDL es muy limitada, por lo que cuando la movilización de ácidos grasos del tejido adiposo es excesiva los NEFA se acumulan dentro del hígado como triglicéridos.
Por otra parte, ante la llegada masiva de NEFA al hígado, éste es incapaz de oxi- dar completamente los NEFA, y una consecuencia de la oxidación parcial de los NEFA es la formación de cuerpos cetónicos que desarrollan potencialmente cetosis. Las estimaciones de la incidencia del síndrome de hígado graso en la vaca de leche varia considerablemente, aunque se apunta una incidencia entre el 35 y 66%; se debe tener en consideración que es muy común que la mayoría de las vacas acumulen una cierta cantidad de grasa en el hígado durante los primeros días del postparto, pero lo que no conocemos es el umbral de la acumulación de triglicéridos hepáticos que da lugar a síntomas de enfermedad en la vaca. Evidencias recientes indican que la acumulación de triglicéridos provoca fallos en la capacidad ureagénica del hígado (la detoxificación natural del amoniaco circulante), lo cual probablemente conduzca también a un fallo en su capacidad gluconeogénica. El resultado neto de este fallo metabólico es la disminución de la ingesta de alimento y la producción de leche, incrementándose la incidencia de enfermedades y disminuyendo el rendimiento reproductivo.
PASOS METABÓLICOS DE LA GRASA EN EL HÍGADO DE LOS RUMIANTES:
1.- OXIDACIÓN.
Los NEFA movilizados por el metabo- lismo llegan al hígado, donde deben ser oxidados o “quemados” para asegurar el aporte de energía a los tejidos; la oxidación de los NEFA en el hígado puede ser dividida en dos fases para una mejor comprensión; la primera es la conversión de los ácidos grasos en un compuesto intermediario, el acylCoA. La segunda fase puede tomar dos rutas en función de la disponibilidad de sustancias en el hígado; la ruta normal o primaria es la reacción del acylCoA con el oxalacetato que da lugar a una oxidación completa con producción de CO2 y gran cantidad de energía; cuando el animal no tiene suficiente cantidad de oxalacetato disponible, el acylCoA es parcialmente oxidado a cuerpos cetónicos, especialmente B-hidroxi- butirato, que es empleado a su vez como fuente de energía alternativa por los tejidos; sin embargo, cuando la cantidad de cuerpos cetónicos es muy elevada tanto por el exceso de oxidación de los NEFA hepáticos como por su oxidación incompleta, éstos se acumulan en sangre dando lugar a la enfermedad por todos conocida como cetosis.
El oxalacetato se obtiene del meta- bolismo del ácido propiónico procedente de la fermentación ruminal de los alimen- tos, o bien a partir de la glucosa almace- nada. Cuando la demanda de energía es muy elevada, la cantidad de ácido propiónico y glucosa disponibles para producir oxalacetato son bajas y se incrementa la ruta cetogénica de oxidación de los ácidos grasos predisponiendo la aparición de cetosis.
2.- SECRECIÓN COMO VLDL.
El hígado de los rumiantes no esta preparado para intercalar simultáneamente las dos funciones de esterificación (“unión”) e hidrólisis (“ruptura”) de grasa después del parto, por lo que los ácidos grasos (NEFA) que llegan al hígado que no son desviados inmediatamente a la ruta oxidativa, serán esterificados a triglicéridos y almacenados en el interior de capacidad de secreción. Esto es lo que sucede en el postparto, los triglicéridos hepáticos se incrementan gradualmente desde el día 1 después del parto y durante las siguientes tres semanas.
La síntesis de VLDL necesita: triglicéridos, fosfolípidos, colesterol, ésteres de colesterol y apolipoproteínas. Los componentes que con más frecuencia se citan como limitantes para la formación de VLDL son los triglicéridos, la apolipoproteína B-100 (ApoB) y la fosfatidilcolina.
a) Triglicéridos: aunque existe una grancantidad de triglicéridos en el hígado, la carencia de enzimas hidrolíticas puede provocar una carencia en su disponibilidad para la formación de VLDL, aunque es posible que existan otros mecanismos capaces de transferir triglicéridos desde los puntos de almacenamiento hasta el lugar de síntesis de VLDL.
b) Apolipoproteina B-100: es necesaria para estabilizar la partícula de VLDL. La interferencia en la síntesis o una mala utilización de la molécula ApoB tendrá un efecto depresor directo en la cantidad de VLDL sintetizada y por tanto en la cantidad de triglicéridos exportados del hígado.
c) Fosfatidilcolina: aunque la mayoría de los animales sintetizan fosfatidilcolina, aquellos alimentados con dietas deficientes en colina y metionina desarrollan hígado graso. El mecanismo de este proceso esta muy ligado a la síntesis de VLDL; recientes trabajos indi- can que la síntesis de fosfatidilcolina es necesaria para la secreción de ApoB en las células del hígado.
MODULACIÓN NUTRICIONAL DEL METABOLISMO DE LA GRASA EN EL HÍGADO
El objetivo de estudiar el metabolismo hepático de las grasas es poder incidir sobre él para manipular su funcionamiento buscando el máximo beneficio para los animales. En el caso concreto de la vaca de leche en fase de transición, este conocimiento metabólico busca prevenir enfermedades tan importantes como la cetosis post-parto y el síndrome del hígado graso, que tienen unas repercusiones económicas tremendas en los actuales sistemas de producción láctea y cuya incidencia es ya muy elevada y la tendencia natural, con vacas cada vez más productoras, es a seguir incrementándose.
Siguiendo los conceptos anteriores, los puntos clave para conseguir un buen metabolismo hepático durante la fase de periparto en la vaca de leche son los siguientes:
1.- Moderar la llegada masiva de NEFA al hígado (evitar una excesiva movilización de grasa).
2.- Conseguir una completa oxidación de los NEFA que llegan al hígado.
3.- Incrementar la eliminación de la grasa almacenada en el hígado, facilitando su exportación como VLDL.
El primer punto es, probablemente, el más importante de todos, puesto que controlando el aporte de NEFA al hígado prevenimos la saturación del mecanismo de oxidación y evitamos un excesivo al- macenamiento de grasa que después debemos exportar. El segundo realmente previene la aparición de la cetosis post- parto y el tercero es clave para paliar el efecto negativo del síndrome del hígado graso, tanto como preventivo como, en cierto modo, curativo.
1.- MODERAR LA LLEGADA DE NEFA:
 La movilización de grasa (lipólisis) con liberación de NEFA a la sangre se produce siempre que el animal necesita energía adicional a la que es aportada por los animales. Es decir, siempre que se encuentre en balance energético negativo (BEN); una vaca entra en BEN cuando produce mucho y es incapaz de ingerir naturalmente todo lo que necesita o bien cuando no recibe comida suficiente o la ración que se le presenta es demasiado baja en nutrientes con respecto a lo que necesita.
La movilización de grasa (lipólisis) con liberación de NEFA a la sangre se produce siempre que el animal necesita energía adicional a la que es aportada por los animales. Es decir, siempre que se encuentre en balance energético negativo (BEN); una vaca entra en BEN cuando produce mucho y es incapaz de ingerir naturalmente todo lo que necesita o bien cuando no recibe comida suficiente o la ración que se le presenta es demasiado baja en nutrientes con respecto a lo que necesita.
En realidad, en los actuales sistemas de explotación, el BEN se presenta casi exclusivamente en el período de transición o periparto (tres semanas antes del parto –preparto- y tres semanas después del parto-postparto-), cuando los niveles de producción se elevan bruscamente y la ingesta esta muy deprimida; en esta fase, de forma totalmente normal, la vaca es incapaz de ingerir lo que necesita y obtiene energía a partir de sus reservas grasas.
En función de la magnitud del BEN, la movilización será mas o menos intensa y el hígado y los tejidos recibirán mayor o menor afluencia de NEFA, y en función del estado del animal (condición corporal, reservas de glucosa, etc) el hígado será capaz de metabolizar mayor o menor cantidad de los NEFA que llegan.
Visto de este modo, la forma más sencilla de evitar problemas hepáticos en el postparto es incrementar los aportes de energía, para lo cual ofrecemos tres alternativas:
ARTICULO COMPLETO METABOLISMO HEPATICO Y VACA EN TRANSICION

